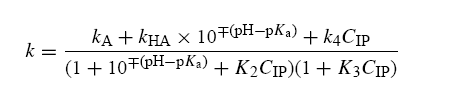Chromatografie iontových párů - principy
Při chromatografii iontových párů se využívá tvorby iontových asociátů mezi separovanými látkami iontové povahy a opačně nabitým iontem, jehož molekula obsahuje relativně velký nepolární podíl. Chromatografie iontových párů má navrženy dva
modely separace - dynamický model iontové chromatografie a mechanismus separace iontových párů. Chromatografie iontových párů je velice silný
nástroj k ovlivnění selektivity separovaných látek iontové povahy, přičemž retence látek neutrální povahy se téměř neovlivní. Retence separovaných látek s opačným nábojem než vlastní protiiont se zvyšuje, retence separovaných látek se stejným nábojem jako vlastní protiiont se snižuje.
Model iontových párů
V tomto modelu se předpokládá vznik iontových párů mezi chromatografovanými disociovanými kyselinami nebo zásadami s opačně nabitými
ionty v mobilní fázi. Vzniklé iontové páry jsou neutrální (hydrofobní) a proto jsou na rozdíl od látek iontové povahy zadržovány na nepolární fázi a vykazují podstatně zvýšenou retenci. Mechanismus vzniku iontových párů lze znázornit:
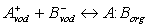
|
a tomuto ději odpovídá rovnovážná konstanta
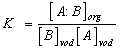
|
a pro distribuční konstantu KD můžeme napsat
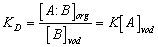
|
Z výše uvedené rovnice je zřejmé, že retence vzniklého iontového páru roste s rostoucí koncentrací protiiontu [A] v mobilní fázi.
Protolyticky lze pro tvorbu iontového asociátu psát:
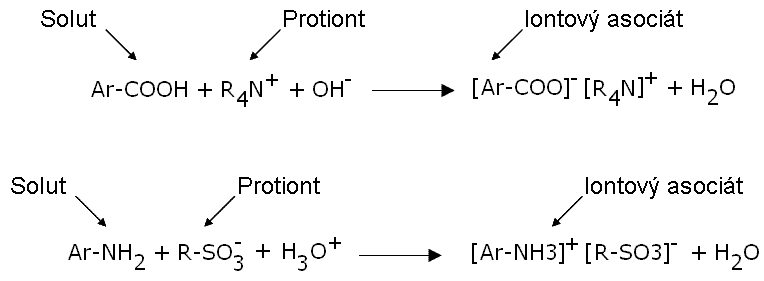
|
Obecně retence závisí na:
- koncentraci protiiontu [1] – pro nízké
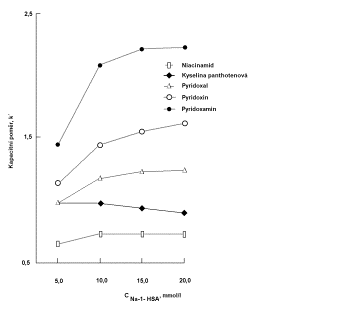
koncentrace protiiontu (do 10 mmol/l) s rostoucí koncentrací protiiontu retence separovaných látek s opačným nábojem roste, pro vyšší koncentrace protiiontu (asi nad 10 mmol/l) s rostoucí koncentrací protiiontu se retence separovaných látek s opačným nábojem vyrovnává a zvýšením koncentrace protiiontu se retence již nemění. Při jaké koncentraci protiiontu dojde k vyrovnání retence závisí na složení mobilní fáze a na délce alkylového řetězce protiiontu. Na obrázku je ukázka separace ve vodě rozpustných vitaminů a vliv na koncentrace hexansulfonové kyseliny na retenci jednotlivých vitaminů. Je vidět, že se rostoucí koncentrací protiiontu retence kationtů
roste (niacinamid, pyridoxal, pyridoxamin, pyridoxin) a aniontu (kyselina panthotenová) klesá. Je zřejmé, že optimální koncentrace protiiontu je asi 10 mmol/l, kdy rozlišení všech separovaných složek je optimální. Při koncentraci protiiontu 5 mmol/l nedochází k separaci pyridoxalu a kyseliny panthotenové.
- velikosti alkylu protiiontu i chromatografovaného iontu (s rostoucí velikostí retence roste)
- iontové sile a pH mobilní fáze.
Nastavení optimálního pH mobilní fáze podporuje disociaci chromatografovaných látek a tím i tvorbu iontových párů. Tato technika tak
otevírá řadu možností pro ovlivnění selektivity dělení chromatografovaných látek. Nevýhodou této techniky je potřeba poměrně dlouhé ustanovení rovnováhy na chromatografické koloně – tzn. potřeba dlouhé doby k ekvilibrace kolony (nejméně 30 kolonových objemů).
Jako iontových párů se používají pro báze silné organické kyseliny (alkansulfonové – pentyl- , hexyl-, heptyl- nebo oktylsulfonové) a pH mobilní fáze se upravuje na hodnotu pH 3-4. Jako protiionty pro kyseliny slouží kvartérní amoniové soli a pH mobilní fáze se upravuje na hodnotu pH 7-8 (tetrabutylamoniumfosfát, cetyltrimethylamoniumsulfát). Pracovní koncentrace protiiontů se pohybuje okolo
5 až 10 mmol/l.
|
Model dynamické iontové chromatografie
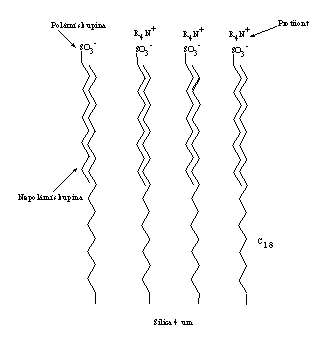
Tento model předpokládá tzv. dynamickou iontovou výměnu (interakci) mezi chromatografovanými látkami iontové povahy s opačně nabitými částicemi protiiontu, který je dynamicky vázán na povrch stacionární fáze, který je dodáván mobilní fází. Model je graficky zobrazen na obrázku.
Obrázek č. 2 Model dynamické iontové chromatografie
|
Isocratickou retence v ion-párové chromatografii je možné pospat rovnicí:[2]
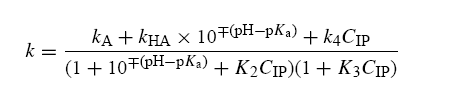
|
kde KHA je retenční faktor kyseliny(nebo báze), KA je retenční faktor ionizované formy (kyseliny nebo báze), k4 je hypotetická retence iontového asociátu díky adsorpci na stacionárná fázi,K2 je rovnovážná konstanta iontového asociátu v mobilní fázi, K3 je rovnovážná konstanta iontového asociátu ve stacionární fázi, CIP je koncentrace ion-párového činidla, pH je pH mobilní fáze a pKa je disociační konstanta solutu.
Literatura
[1] Knox J.H., Hartwick R.A.: J. Chromatogr. 204 (1981) 3.
[2] Jianwei Li: Anal. Chim. Acta 522 (2004) 113-126.
Last modified:
![]()
![]()
![]()
![]()