Robustnost metody
Anglický ekvivalent pro robustnost je Ruggedness nebo Robustness. První zmínka o robustnosti – Youden (1961): "… analytical process need to be „rugged“…
Robustnost analytického postupu je mírou jeho kapacity zůstat netečný vůči malým, ale záměrným změnám parametrů metody a poskytuje informaci o jeho spolehlivosti během běžného používání.
Robustnost je tudíž schopnost metody být „netečná k mírným (a nevyhnutelným) odchylkám od některé obvyklé rutinní činnosti“ (W.J. Youden, Statistical techniques for collaborative tests. Statistical manual of the AOAC, Washington DC.
Dále může být robustnost definována jako míra vlivu mírného kolísání úrovně jednotlivých parametrů na výsledek analytického stanovení. Definice robustnosti je v každém protokolu jiná (ICH, FDA, PhEur, JP, USP). Srozumitelná definice je následující: Robustnost metody je definována jako míra kapacity metody při jejím reprodukování za nepatrně změněných podmínek. Změna podmínek může nastat pro případ mezilaboratorních zkoušek (jiná laboratoř, analytik, instrument = RUGGEDNESS) nebo změnou podmínek v jedné laboratoři (teplota, koncentrace, doba extrakce = ROBUSTNESS).
Zde si dovolím nadefinovat svou vlastní verzi: Robustnost metody je taková vlastnost metody, kdy malou změnou jejich parametrů, poskytuje metoda pořád správné a přesné výsledky.
Největší problém při ověřování robustnosti podle výše uvedených definic je definování míry (velikosti) odchylky (parametru) resp. mírného kolísání úrovně. Nebyla stanovena žádná kriteria (velikost odchylky), ale obecně by se mělo vycházet z nejistoty měření nebo předpisů (PhEur, JP, USP).
Co je cílem resp. výsledkem ověření robustnosti metody? Výsledkem není závěr, že metoda je robustní nebo nerobustní, ale výsledkem robustnosti je informace, jaké parametry metody jsou kritické vyžadující pečlivou kontrolu. Výsledkem robustnosti může být také interval kritických parametrů metody, ve kterém metoda poskytuje nejmenší chyby měření.
Při ověřování robustnosti existují dva zásadní přístupy k tomuto problému: univariační (jednorozměrná) analýza dat nebo tzv. multivariační (vícerozměrná) analýza dat.
Univariační (jednorozměrná) analýza dat
Postup: Mění se jeden parametr (faktor) v čase a ostatní parametry (faktory) zůstávají fixní a sleduje se jak ovlivní výsledek. Poté se experiment zopakuje s dalším parametrem – tzv. přístup OFAT (One Factor At Time).
Příklad: Nechť máme 3 parametry (A,B,C) a sledujeme pouze dva extrémy každého parametru: (-) a (+) a ostatní zůstávají neměnné (0) atd …, pak metodou OFAT dostaneme následující kombinace:
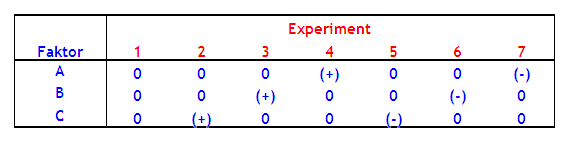
|
Pro počet experimentů obecně platí: 2*k+1. Mluvíme o tzv. hvězdicovém schématu („
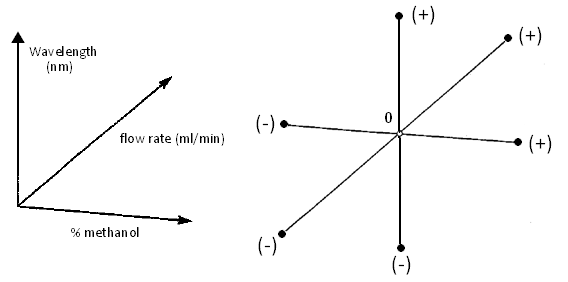
|
Další z používaných algoritmů je tzv. zrcadlové faktorové schéma („
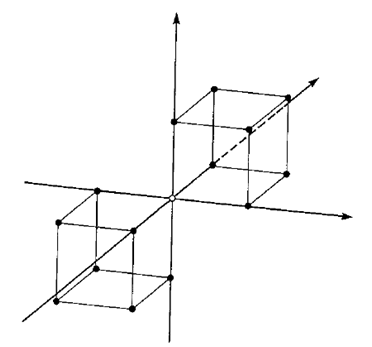
|
Pro počet experimentů obecně platí: 2*(2k+1) a dostáváme následující kombinace:

|
Multivariační (vícerozměrná) analýza dat
Robustnost metody vůči malým změnám se testuje na základě plánovaných pokusů (úplných nebo zkrácených).
Příklad: Pro jednoduchost = výsledek ovlivní pouze dvě proměnné veličiny (např. teplota a čas; veličiny mohou být plynule měnitelné nebo i binární). Při experimentu převádíme všechny proměnné na binární: + a – (u plynule proměnných tedy volíme dva stavy: nominální a extrémní a počet úrovní proměnné veličiny je tedy 2). Plán pak lze popsat takto:
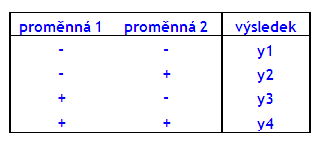
|
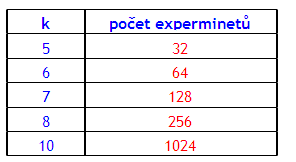
Velice časově náročné, v případě že chceme sledovat vliv 4 proměnných pak dostaneme 24 = 16 experimentů, které je nutné udělat. Obecně platí: 2k. Nárůst poštu experimentů je patrný z tabulky:
|
Při optimalizaci postupu pro silanizaci silikagelu pro HPLC museli autoři posoudit 23 proměnných. V případě, že by jeden experiment trval 10 minut, pak k provedení úplného plánu bylo zapotřebí 160 let nepřetržité práce.
Z důvodu takto velkých počtů experimentů se zanedbává možnost ovlivňování jednotlivých proměnných => tzv. neúplné faktorové plány (fiktivní proměnné) s různými algoritmy. Postup pro testování pomocí Plackett-Burmanova plánu je popsán zde.
Existuje ještě řada dalších postupů a algoritmů hodnocení, pro úplnost uvádím Dongův, Vander Heydenův, Youdenův algoritmus.
- Jones K., J. Chromatogr. 392 (1987) 1.
- Plackett R.L., Burmann J.P., Biometrika 33 (1946) 305.
- M. Mulholland, TRAC, 7 (1988) 383.
- Y. Vander Heyden, F. Questier and D.L. Massart, J. Pharm. Biomed. Anal. 8 (1998) 43.
- van de Vaart F.J. et al., Het Pharmaceutisch Weekblad 127 (1992) 1229.
- M. Mulholland, J. Waterhouse, J. Chromatogr. 395 (1987) 539.
- Y. Vander Heyden, C. Hartmann, D.L. Massart; L. Michel, P. Kiechle, F. Erni, Anal. Chim. Acta 316 (1995) 15.
- Y. Vander Heyden, F. Questier, D.L. Massart, J. Pharm. Biomed. Anal. 17 (1998) 153.
- Y. Vander Heyden, D.L. Massart; Y. Zhu, J. Hoogmartens, J. De Beer; J. Pharm. Biomed. Anal. 14 (1996) 1313.
- Y. Vander Heyden, C. Hartmann, D.L. Massart, P. Nuyten, A.M. Hollands, P. Schoenmakers, J. Chromatogr. A 756 (1996) 89.
- Y. Vander Heyden, M. Jimidar, E. Hund, N. Niemeijer, R. Peeters, J. Smeyers-Verbeke, D.L. Massart, J. Hoogmartens, J. Chromatogr. A, 845 (1999) 145.
- ICH Harmonised Tripartite Guideline prepared within the Third International Conference on Harmonisation of Technical Requirements for the Registration of Pharmaceuticals for Human Use (ICH), Validation of Analytical Procedures : Methodology, 1996, 1-8.
- Youden W.J., Mater. Res. Stand. 1 (1961) 863.
Last modified:






